NaOH (Sodyum hidroksit) ve Su Tepkimesi:
Sodyum hidroksit, suya karıştırıldığında iyonlarına ayrışır ve bu ayrışma sonucunda bazı değişiklikler meydana gelir. Bu tepkime şöyle açıklanabilir:
NaOH suda çözünür:
NaOH, suya karıştığında sodyum iyonu (Na⁺) ve hidroksit iyonu (OH⁻) olarak ayrışır.
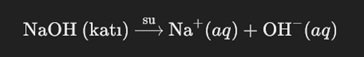
Hidroksit iyonları (OH⁻) su içinde bazik özellik gösterir. Yani, hidroksit iyonları suya karıştığında suyun pH’ını artırır, bu da çözeltinin alkali (bazik) olmasına neden olur.
pH nedir?: pH, bir çözeltinin asidik ya da bazik olduğunu gösteren bir ölçektir. pH değeri 7’den küçükse asidik, 7’den büyükse baziktir.
NaOH çözeltisi bazik bir çözelti oluşturur, çünkü hidroksit iyonları (OH⁻) suyun içinde serbestçe hareket eder.
Sonuç:
NaOH, suya karıştığında hidroksit iyonları (OH⁻) açığa çıkar ve bu çözeltinin bazik olmasına yol açar.
Bu tür çözeltiler, asidik maddelere karşı tepkime gösterir ve nötralizasyon reaksiyonları oluşturabilir.
Örnek: Eğer bu çözeltinin içine bir asit (örneğin HCl, hidroklorik asit) eklersek, OH⁻ iyonları ile H⁺ iyonları birleşerek su ve tuz (NaCl) oluşturur. Bu, nötralizasyon reaksiyonudur.
